Au démarrage du développement d’un Dispositif Médical (DM), les questions suivantes se posent :
- Doit-on réaliser une analyse de risques pour chaque variante d’une même gamme de produit ?
- Mais comment suivre et mettre à jour les risques communs à toute la gamme ?
- Et comment identifier les spécificités de certaines variantes ?
- Sur quoi portent ces spécificités ?
- Sur l’événement initiateur / le danger ?
- Sur le dommage ?
- Sur la mesure de réduction du risque ?
Notre module logiciel ISO 14971 vous apporte une réponse opérationnelle :
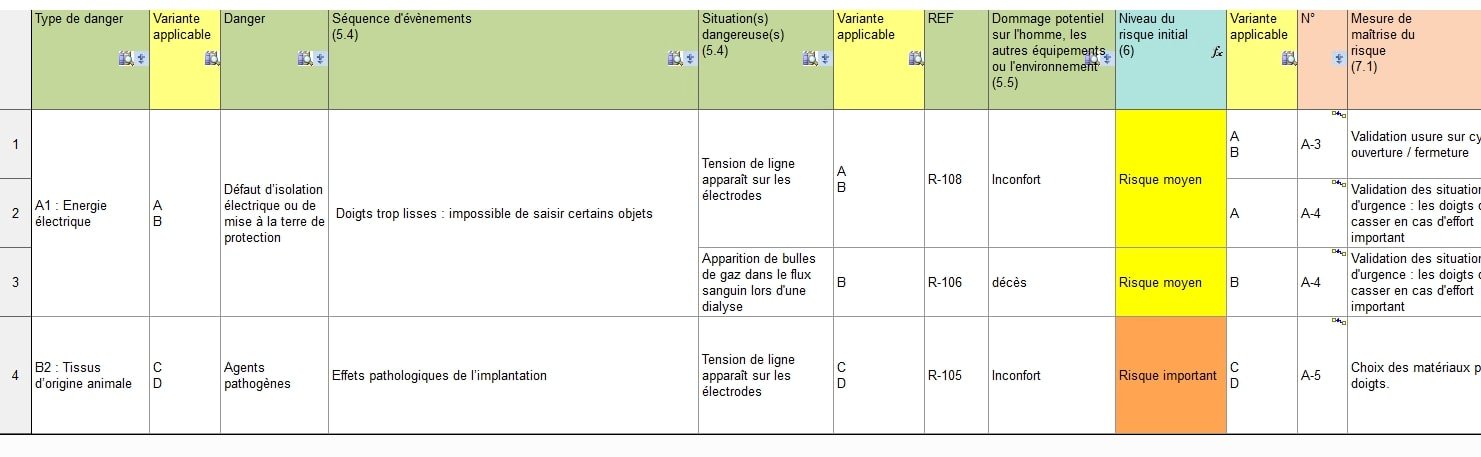
Pour chaque étape de l’analyse (identification des dangers, des dommages et des mesures de réduction des risques), il est possible de sélectionner la ou les variantes concernées :
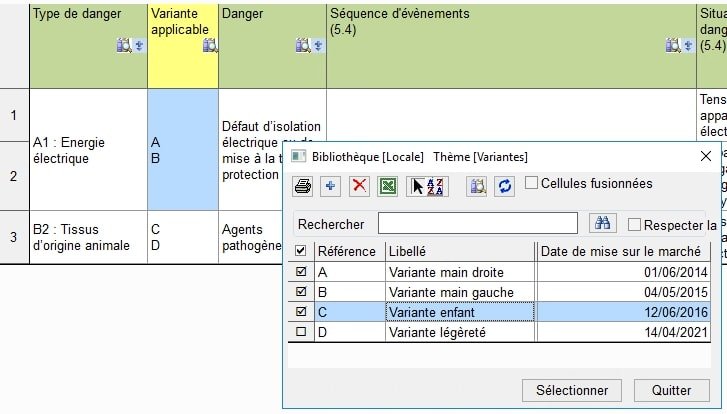
À chaque variante vous pouvez associer une date de mise sur le marché afin de gérer de manière spécifique le suivi post marché associé à chaque variante.
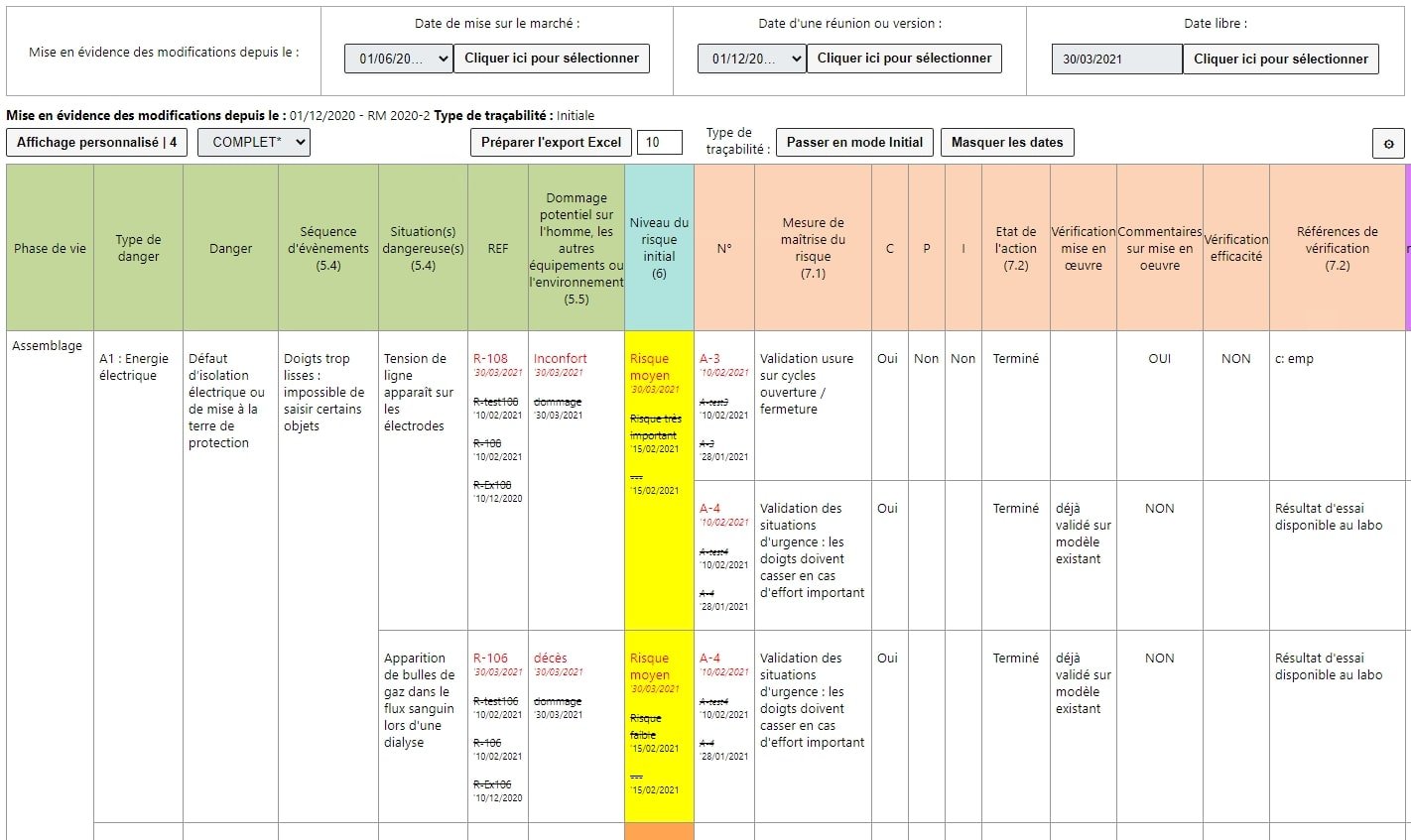
Un rapport vous permet également de mettre en évidence les modifications effectuées sur une variante donnée après la mise sur le marché.
- Une analyse de risques s’applique pour toute une gamme de produits
- Les spécificités de chaque variante sont rigoureusement analysées
Les rapports peuvent aussi bien être édités pour la famille de produits que pour une référence ou une variante.